by Inge Heinzl, Marisabel Caballero, Ajay Bhoyar, EW Nutrition
あなたの運営から壊死性腸炎を排除するには、それが何であるか、予防方法、および家禽生産への影響を軽減する方法について十分に理解することから始まります。
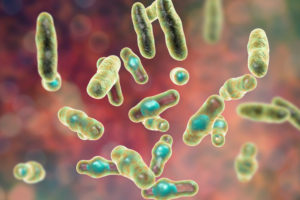
壊死性腸炎は、小腸でClostridium perfringens A型およびC型の過剰増殖によって引き起こされる家禽疾患です。C.perfringens によって産生される毒素は、腸壁に損傷を与えます。一般に、2〜6週齢のブロイラーで起こります。無症状型では、消化管の障害を特徴とします。臨床形態は、非常に短時間で深刻な問題をもたらし、同群での死亡率を増加させます。
壊死性腸炎は、世界的な家禽生産において年間60億ドルの損失の原因で、この疾患は増加傾向にあります。その理由の1つは、動物生産において抗生物質の自主的または法的義務による削減によるためです。この傾向は、抗菌剤耐性の増加および消費者の需要によって推進されています。もう一つの理由は、コクシジアの増殖に加えて、クロストリジウムに対しても有効性を示すイオノフォアの使用減少です。抗コクシジウム生ワクチンを使用する場合、これらのイオノフォアの使用ができず、クロストリジウム/壊死性腸炎が増加します (Williams, 2005)。
これはすべての家禽で広範な問題ですが、特にブロイラーにとって、壊死性腸炎およびコクシジウム症は最も重要な健康問題です。
壊死性腸炎(NE)の症状および無症状疾患
症状
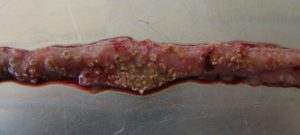
急性の黒っぽい下痢によって濡れた敷き藁を発見し、最初の臨床徴候が現れた後、突然1日あたり最大1%の集団死亡率の上昇を特徴とします(Ducatelle, 2010)。死亡率は時々50%まで上昇します(Van der Sluis, 2013)。鶏は汚れた羽毛、無気力、食欲不振が見られます。
典型的な壊死は、粘膜表面が荒れ、病変、および茶色っぽい(ジフテリア様)疑似膜を有する膨らんだ小腸を示します。死後の検査では、大量の水っぽい茶色で、血が混ざった液体で、悪臭があります。肝臓は黒く腫れて堅くなり、胆嚢は膨満します (Hofacre, 2018)。
過急性壊死性腸炎の場合、鶏は初期症状を示さずに死亡することがあります。
無症状疾患

鶏が無症状なのに苦しむ場合、腸粘膜の慢性的な損傷と小腸内の粘液量の増加は、栄養素の消化と吸収の障害につながり、成長が悪くなります。
劣化した飼料への変換とその結果生じる成長の低下は、35日齢頃に顕著になります。飼料がブロイラー鶏の生産コストの約 65~75%寄与するため、飼料変換が不十分であると、生産コストが増加し、収益性に大きく影響します。しばしば、明確な症状の欠如のために、この無症状疾患は未治療のままであり、生産効率に恒久的に影響を与えます。
病原体
壊死の原因は、グラム陽性嫌気性細菌のClostridium perfringens A型の特定の株と、一部のC型株です(Keyburn, 2008)。
クロストリジウムは、主に有機物質が分解される土壌、下水、動物やヒトの胃腸管で増殖します。これらの細菌は、いくつかの消毒剤と同様に、環境への影響(熱、照射、排除)にも非常に耐性があり、数年間生存することができます。適切な条件下では、 C.perfringensの芽胞は飼料や敷き藁で増殖することさえあります。
C.perfringensは、鶏の腸の常在菌です。健康な鶏では、消化管で102~104 CFU/gあり多種多様な細菌の混合物中に生存しています (McDevittet, 2006)。この疾患は、通常、高タンパク質、低免疫、および腸内細菌叢の不均衡などの要因の組み合わせにより小腸で急増したときに発症します。その後、菌数は消化管で107~109 CFU/gに上昇します。(Dahiya, 2005)
壊死性腸炎B毒素(NetB);壊死性腸炎(NE)にとっての重要な病原性因子
宿主で立証するために、 Clostridium 属および他の病原体は、病原性因子に依存します(インフォボックスを参照)。これらの病原性因子には、例えば、宿主の免疫系への付着、回避または抑制のための「手段」、栄養素を得るための「手段」、腸細胞への侵入のための「手段」などがあります。長年にわたり、C.perfringens によって産生されるα毒素は、この疾患の発症および主要な病原性因子に関与すると仮定されていました。2008年Keyburnは、αトキシンを産生しないが、壊死性腸炎を引き起こす C.perfringens 変異株を使用することによって、別の重要な病原性因子を発見しました。
それで、壊死性腸炎に罹患している鶏にのみ存在する別の毒素が同定されました。C.perfringens壊死性腸炎B毒素(NetB)です。NetBは孔形成毒素です。孔形成毒素は、通常病原菌によって産生される外毒素で、他の微生物によって産生される場合もあります。これらの毒素は、腸壁細胞膜の高潔を破壊します。漏れた細胞の内容物は、細菌のための栄養素として使用されます。免疫細胞が破壊されると、免疫反応が部分的に影響を受ける可能性があります(Los, 2013)。
さらに、C.perfringensの病原性株はバクテリオシンを産生します。— 最も重要なのはPerfrinです(Timbermont, 2014)。— 無害なClostridium属の増殖を抑制し、鶏の正常な腸内細菌叢を置き換えます (Riaz, 2017)。
病原性因子の例
1.接着因子
病原体がターゲットホストサイトに付着または付着できるようにします(例:繊毛)。繊毛は、病原体間のRNAまたはDNAの交換を可能にします。
2.侵入因子
宿主組織内の病原体の侵入および分布を促進する(侵入と拡散酵素)。例えば:ヒアルロニダーゼは、病原体が積極的に移動することを可能にする結合組織または鞭毛のヒアルロン酸を攻撃します。
3.毒素
宿主細胞の機能を損傷するか、それらを破壊します(例:エンドトキシン-リポ多糖類、外毒素)
4.回避の戦略
病原体が免疫系の防御戦略を受けることを可能にします(例えば、抗食作用因子は食細胞による攻撃に対する防御を提供します。特異的抗体は酵素によって不活性化されます)。
最適な健康の腸を持つ鶏は、壊死性腸炎の影響を受けにくいかもしれません。栄養原を割り当て、腸の環境をこれらの病原体が増殖に適したものにしても、それらが病気を引き起こすことを可能にするためには、追加の要因が必要です(Van, 2008; Williams, 2005)。
素因
飼料:組成と粒子サイズ
壊死性腸炎の発症における飼料の役割を過小評価してはなりません。これは、 C.perfringens に有利な腸内環境を作成する物質が活動に関与してくるところです。
NSps(非デンプン多糖類)
作用機序
-粘度を上げる
-透過率を下げる C.perfringensが利用できる多くの栄養素
-他の栄養素の消化率を下げる
-栄養素を提供する
粘液産生の刺激 嫌気的環境
(Van, 2013、Kaldhusdal, 1996、Annett, 2002)
タンパク質と脂質
タンパク質の過剰な含有量
難消化性タンパク質
魚粉のような特別な高タンパク質 腸内菌層のバランスの変化
亜鉛/グリシンの濃度 (Antonissen, 2016)
作用機序
-消化管における高タンパク質のレベル
-細菌の栄養素として利用
動物性脂質
作用機序
- 高いpHと高い胆汁塩濃度 C.perfringensの増加
- 球菌の増殖 (Knarreborg, 2002)
粒径
粒径が均一でない 壊死性腸炎の増加率
(Branton, 1987)
細く砕く
作用機序 病原微生物の増加
- 砂嚢の筋肉組織↓ (Salmonella, Campylobacter, Clostridium…)
- pH↑、消化管通過時間↓ (粗いトウモロコシと比較して)
(Rougiere, 2010; Santos, 2008; Singh, 2014)
マイコトキシン汚染
マイコトキシンは消化器官に害を及ぼし、C.perfringensの増殖に理想的な条件を作り出します 。
マイコトキシンは、C.perfringens増殖、毒素産生、またはNetB産生に直接作用しません。しかしながら、マイコトキシンは消化器官を破壊し、病原体にとって好ましい環境を作り出します。たとえば、次のようになります。
- デオキシニバレノール(DON)は、腸障壁を破壊し、上皮を損傷することによって、C.perfringensの増殖のための良好な条件を提供します。おそらく結果として生じる上皮の透過性および食物タンパク質の吸収の低下は、小腸におけるタンパク質の増加をもたらす可能性があります。これらのタンパク質は、病原体の栄養素として役立つ可能性があります (Antonissen, 2014)。
- デオキシニバレノール(DON)および他のマイコトキシンは、乳酸産生細菌の数を減少させ、微生物バランスを変化させます (Antonissen, 2016)。
アイメリア属
無傷の腸上皮は、C.perfringensなどの潜在的な病原体に対して最良の防御です。ここでは、コクシジウム症について説明します。Moore(2016)は、腸上皮を損傷することにより、アイメリア属は粘膜上皮の腸基底領域への侵入をC.perfringensに与えることを示しました。その後、病理学的プロセスの第1段階が行われ、そこからC.perfringens が固有層に侵入します。上皮の損傷が続きます (Olkowski, 2008)。腸に漏れる血漿タンパク質と産生される粘液は豊富な栄養源です(Van、2004; Collier、2008)。 コクシジウム症のさらなる影響は、生来の免疫防御を活性化する Candidatus savagellaの数を減らすことによって、腸内の微生物バランスを変化させることです。
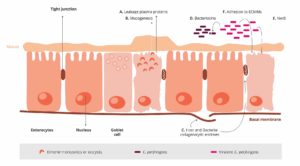
- アイメリア は上皮細胞を殺傷して血漿タンパク質の漏出を誘発します。
- それらは腸内の粘液産生を増強にします。
1+2は、利用可能な栄養素の増加をもたらし、C.perfringens の増殖に有利な環境を作り出します。
アイメリア 属だけでなく、他の病原体(例えば サルモネラ属、アスカリッド幼虫、ウイルス)や腸粘膜に損傷を与えるマイコトキシンなどの物質は、C.perfringens感染のための道を開くことができます。アイメリア属の卵母細胞の発散に不可欠な湿気のような素因も、壊死性腸炎の促進因子として考慮されなければなりません。(Williams、2005)。
免疫抑制因子
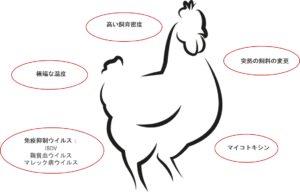
すでに説明されているインフルエンサー飼料、マイコトキシンおよびコクシジアに加えて、他の素因も言及されなければなりません。一般に、動物にストレスを誘発する要因は、腸内細菌叢のバランスを崩します。結果として生じる免疫系の抑制は、壊死性腸炎のリスクに寄与します(Tsiouris, 2016)。これらの要因は次のとおりです。
細菌 :Shivaramiaah(2011)は、壊死性腸炎素因として新生児Salmonella typhimurium感染を調査しました。早期感染は、腸に重大な損傷を引き起こします(Porter, 21)。さらに、Hassan(1994) は、S.typhimuriumの感染がリンパ球の発生に悪影響を及ぼし、C.perfringensのコロニー形成を促進する可能性があることを示しました。
ウイルス :伝染性ファブリキウス嚢病(IBD)は、サルモネラ、ブドウ球菌だけでなく、クロストリジウムによる感染の重症度を増加させることが知られています。他のクロストリジウムを促進するウイルス性疾患としては、ガンボロ病やマレック病があります。
ストレス :腸管は、あらゆるタイプのストレスに特に敏感である。このストレスは、高温、高密度、飼料供給の急激な変化などによって引き起こされる可能性があります。
治療
急性の場合、農家は獣医師に相談し、鶏を治療する必要があります。
処理は飼料または飲水で行われるため、飲水または飼料を消費する鶏のみが処理されることに言及する必要があります。
抗生物質
グラム陽性菌を標的とする抗生物質は、急性壊死性腸炎の治療に一般的に使用されます。抗生物質の選択は、飼育様式および農場/群れにおける抵抗遺伝子の存在を考慮して、獣医師によって対処されなければなりません。
抗生物質の予防的使用は推奨されておらず、多くの国はすでに抗菌剤耐性(AMR)を低減するためにそれを禁止しています。
抗菌剤耐性(AMR)
いくつかの細菌は、遺伝子変異のために特定の抗生物質に対する感受性が低くなっています。次のことが可能です。
- 抗生物質を分解または改変してそれらを不活性化する酵素の産生を刺激します(1)。
- 抗生物質の入口をなくすか、または効果を発揮す前に抗生物質を放出するポンプの開発を促進します(2)。
- 抗生物質が結合する分子(抗生物質のターゲット)を変更または除去する。
これは、対応する抗生物質が使用されると、これらの抗生物質に対する耐性細菌が生き残ることを意味する。競合相手が排除されているという事実のために、彼らはより良い増殖することができます。
さらに、この耐性は「耐性遺伝子」によって伝達される可能性があります。
- ドータセルに
- 死んだ細菌からの摂取経由 (3)
- 水平遺伝子移転 (4)
- ウイルスを通して (5)
抗生物質のあらゆる適用は、抵抗性の発達を促進します(Robert, 2019)。短期間の使用、により良い生物安全性、または低用量での適用は、細菌に適応するより良い機会を与えます。
バクテリオファージ
ファージ治療の実験的使用は、疾患の進行および壊死性腸炎の症状を軽減するのに有効であることが示されています (Miller, 2010)。バクテリオファージカクテルの経口適用により、Millerは、未処理の群と比較してC.perfringens感染ブロイラーで92%死亡率を低減することができました。
作用モード:バクテリオファージによって産生される高度に進化した酵素であるエンドリシンは、ファージ前代放出のために細菌細胞壁を消化することができます(Fischetti, 2010)。しかし、ファージ治療はまだEFSAによって承認されていません。
予防
病気を予防することは、常に良く、より費用対効果が高いです。
それでは、どのように行うべきですか?
C.perfringensの増殖を支持する条件を防止し、宿主の免疫応答を強化することは、疾患の確率を低下させられます。
素因を排除することに加えて、主な目標は次のとおりです。
- 腸内細菌叢のバランス
- 腸機能および完全性の最適化
- 免疫の維持
バイオセキュリティ
壊死性腸炎に罹患している鶏から単離されたClostridium株のほとんどは、実験的にこの疾患を誘発する可能性があり、健康な鶏から単離された株はできないという証拠があります。これにより、特定の株のみが問題であることが確認されました(Ducatelle, 2010)。
したがって、これらの病原性株を農場内に入れないが最も重要です。
- 厳格な バイオセキュリティ対策!
- 各鶏舎の衣類、ブーツ、手洗い/消毒設備を分けておく
- 新しい鶏群の導入で14日以上の空舎期間を設ける
コクシジウム症に対する具体的な対策
- ワクチン接種
寄生虫学者によると、ニワトリには7~9種のアイメリアが見つかっており、互いに交差がありません。効果的なワクチン接種は、最も重要な病原性アイメリア種(E.acervulina、E.maxima、E.tenella、E.necatrix、E.brunetti)の胞子形成オーシストを含まなければなりません。ワクチンに含まれる種が多いほど良いです。しかし、正しい方法を適用しない場合、ワクチンは効果がないか、壊死性腸炎につながる可能性のある鶏を発生させる可能性があります(Mitchell, 2017)。
- 抗コクシジウム剤
耐性の発達を防ぐには、異なる作用様式を有する化学物質(合成化合物)およびイオノフォア(ポリエーテル系抗生物質)交互に使用することが重要です。
イオノフォアには、特定の作用機序があり、鶏に感染する前にオーシストを殺します。イオノフォア分子は非常に小さいため、スポロゾイトの外膜に取り込まれて拡散する可能性があります。そこで、それは濃度勾配を減少させ、スポロゾイト内の水の蓄積を引き起こし、その破裂を引き起こします。
ダイエット
穀物中の非デンプン多糖類(NSP)の最小化

C.perfringensの「摂食」を防ぐには、小麦、小麦副産物、大麦などの水溶性であるが難消化性の非デンプン多糖類(NSP)の高い含有量を避けるか、少なくとも最小限に抑える必要があります。さらに、キシラナーゼを飼料配合に含めることで、NS非デンプン多糖類(NSP)の有害な影響を低減し、飼料エネルギー利用率を改善する必要があります。これらの穀物の代わりに、トウモロコシを飼料に含めることが可能性です。これは、エネルギー含有量が高く、栄養素の利用が高いため、ブロイラーの飼料に最適な成分と考えられています。
低タンパク/高消化性アミノ酸を含む飼料処方
結晶性アミノ酸を補給した低タンパク飼料を与えることは、壊死性腸炎のリスクを低減するのに有益である可能性があります(Dahiya, 2007)。タンパク質の消化率を改善し、C.perfringensの増殖を減少させるために、プロテアーゼを飼料に添加することができます。
食事中の動物性脂肪の回避/最小化
動物性脂肪は、C.perfringens菌の数を増やす傾向があります。したがって、それらは植物性脂肪源に置き換える必要があります。
飼料形状
飼料形態に関しては、Engberg(2002) は、ペレット飼料を与えた鶏は、マッシュ飼料を与えた鶏よりも盲腸と直腸でC.perfringens菌の数が減少したことを発見しました。Branton(1987)は、ハンマー粉砕飼料よりもローラーミル加工飼料(粗粉砕)を供給することにより、死亡率が低いことを報告しました。
添加剤
添加剤は、C.perfringensの増殖を防ぐため、またはC.perfringensの増殖を防ぐ方法で環境条件を変更するために使用することができます。
プロバイオティクス
これらの生きた微生物サプリメントは、腸内微生物叢を確立、維持または再確立するのに役立ちます。
作用機序:
- 基質と付着部位を求めて病原菌と競合する
- 病原菌の増殖を抑制する抗菌物質を産生する (Gillor, 2008)
- エンテロトキシンを結合して、中和する(Mathipa, 2017)
宿主の免疫機能を促進する (Yang, 2012)
プレバイオティクス
-
- これらの飼料成分は、腸内の有益な細菌を増殖するための栄養素として機能します。
作用機序:
- Dマンノースまたはフルクトース、鶏によって消化されないデンプンは、腸内細菌叢の「良い」成長および活性を選択的に促進します。
- フルクトオリゴ糖は、腸内のC.perfringensおよび大腸菌を減少させ、Lactobacillus属を増加させます。(Kim, 2011)
- ガラクトオリゴ糖は、ラクティスベースのプロバイオティクスと組み合わせて、Bifidobacterium属の増殖を選択的に促進することが報告されています(Jung, 2008)。
有機酸
有機酸は、腸の健康を改善するために、動物の飼料によく使用されます。
作用機序:
- pH低下は、有益な細菌が増殖します
- カプリル酸は、C.perfringensを抑制するだけでなく、グルコースの利用を阻害することにより、サルモネラ属も阻害します(Skrivanova, 2006)。
ラウリン酸、クエン酸、オレイン酸、リノール酸、中鎖脂肪酸(C8-C14)は、C.perfringensの 増殖を妨げます。
植物分子
植物分子は、何世紀にもわたって病原体に対して使用されてきました。一般に、これらの物質の2つのサブグループは、C.perfringensに対して有効であることが知られています。
タンニン
- 多くの研究では、蠕虫、アイメリア、ウイルス、細菌などのさまざまな病原体に対するタンニンの有効性が示されています。
- 栗とケブラコの木からの抽出物は、C.perfringensだけでなく、その毒素に対しても有効です (Elizando, 2010)。
- 壊死性腸炎の2つの素因であるアイメリアとサルモネラ属に対するタンニンの活性(Ce, 2011)。
エッセンシャルオイル
-
- それらの疎水性特性により、C.perfringens菌の膜の脂質と相互作用することができます。
- それらは細菌の膜に組み込まれ、その完全性を破壊する可能性があります。
- これにより、イオンやATPなどの他の小分子に対する細胞膜の透過性が高まり、細胞膜上の電気化学的勾配が減少し、細胞の同等のエネルギーが失われます。
Clostridium属への直接的な効果に加えて、多くの植物分子は腸の健康を改善し、Clostridium属の増殖と壊死性腸炎を防ぐのに役立ちます。
マイコトキシン/細菌性毒素結合剤
これらの結合剤には、次の 2 つの作用モ機序があります。
- マイコトキシンの結合、腸上皮の損傷を軽減または防止することができるので、Clostridium増殖の前提条件が生成されません。
- C.perfringensによって産生される結合毒素は、病変の発生または重症度を軽減することができます。:
α-トキシン、ホスホリパーゼCは、膜リン脂質を加水分解し、赤血球、白血球、筋細胞、内皮細胞に損傷を与え、それらの脂肪分解を引き起こします (Songer, 1996)。これは壊死と組織の損傷をもたらします。
- 主要な病原性因子であるNetB毒素の結合は、壊死性腸炎の重症度を軽減する可能性があります。
結論
抗生物質とイオノフォアの使用が減少する傾向は、家禽生産における壊死性腸炎の発生率の増加に貢献しています。
無症候性の壊死性腸炎は一般的に気づかないため、飼料効率が低下し、家禽生産者にとって経済的損失の大きな原因となります。
最適な腸の健康状態を維持することは、壊死性腸炎の発生を防ぐための鍵となります。抗生物質を含まない家禽生産の時代では、この壊滅的な疾病を制御するために、この病原細菌に対してもその素因に対して作用する代替手段を検討する必要があります。

References
Annett, C.B., J. R. Viste, M. Chirino-Trejo, H. L. Classen, D. M. Middleton, and E. Simko. “Necrotic enteritis: effect of barley, wheat and corn diets on proliferation of Clostridium perfringens type A.” Avian Pathology 31 (2002): 599– 602. https://doi.org/10.1080/0307945021000024544
Antonissen G, F. Van Immerseel, F. Pasmans, R. Ducatelle, F. Haesebrouck, L. Timbermont, M. Verlinden, G.P.J. Janssens, V. Eeckhaut, M. Eeckhout, S. De Saeger, S. Hessenberger, A. Martel, and S. Croubels. “The mycotoxin deoxynivalenol predisposes for the development of Clostridium perfringens-Induced necrotic enteritis in broiler chickens. PLoS ONE 9 no. 9 (2014): e108775. https://doi.org/10.1371/journal.pone.0108775
Antonissen, G., V. Eeckhaut, K. Van Driessche, L. Onrust , F. Haesebrouck, R. Ducatelle, R.J. Moore, and F. Van Immerseel. “Microbial Shifts Associated With Necrotic enteritis.” Avian Pathol. 45 no. 3 (2016): 308-312. https://doi.org/10.1080/03079457.2016.1152625
Branton, S.L., F.N. Reece, and W.M. Hagler. “Influence of a wheat diet on mortality of broiler chickens associated with necrotic enteritis.” Poultry Sci. 66 (1987): 1326-1330. https://doi.org/10.3382/ps.0661326
Cejas, E., S. Pinto, F. Prosdócimo, M. Batalle, H. Barrios, G. Tellez, and M. De Franceschi. “Evaluation of quebracho red wood (Schinopsis lorentzii) polyphenols vegetable extract for the reduction of coccidiosis in broiler chicks.” International Journal of Poultry Science 10 no. 5 (2011): 344–349. https://doi.org/10.3923/ijps.2011.344.349
Collier, C.T., C.L. Hofacre, A.M. Payne, D.B. Anderson, P. Kaiser, R.I. Mackie, and H.R. Gaskins. “Coccidia-induced mucogenesis promotes the onset of necrotic enteritis by supporting Clostridium perfringens growth.” Veterinary Immunology and Immunopathology 122 (2008):104–115.
https://doi.org/10.1016/j.vetimm.2007.10.014
Dahiya, J.P., D. Hoehler, A.G. Van Kessel, and M.D. Drew. “Effect of different dietary methionine sources on intestinal microbial populations in broiler chickens.” Poultry Science 86 (2007):2358–2366
https://doi.org/10.3382/ps.2007-00133
Dahiya, J.P., D. Hoehler, D.C. Wilkie, A.G. van Kessel, and M.D. Drew. “Dietary glycine concentration affects intestinal Clostridium perfringens and Lactobacilli populations in broiler chickens.” Poultry Science 84 no.12 (2005):1875-85. https://doi.org/10.1093/ps/84.12.1875
Diaz Carrasco, J.M., L.M. Redondo, E.A. Redondo, J.E. Dominguez, A.P. Chacana, and M.E. Fernandez Miyakawa. “Use of plant extracts as an effective manner to control Clostridium perfringens induced necrotic enteritis in poultry.” BioMed Research International (2016): Article ID 3278359. https://dx.doi.org/10.1155/2016/3278359
Ducatelle, R. and F. van Immerseel. “Necrotic enteritis: emerging problem in broilers.” WATTAgNet.com – Poultry Health and Disease (April 9, 2010).
https://www.wattagnet.com/articles/5523-necrotic-enteritis-emerging-problem-in-broilers
Elizondo, A.M., E.C. Mercado, B.C. Rabinovitz, and M.E. Fernandez-Miyakawa. “Effect of tannins on the in vitro growth of Clostridium perfringens.” Veterinary Microbiology 145 no. 3-4 (2010): 308–314. https://doi.org/10.1016/j.vetmic.2010.04.003
Engberg, R.M., M.S. Hedemann, and B.B. Jensen. “The influence of grinding and pelleting of feed on the microbial composition and activity in the digestive tract of broiler chickens.” · British Poultry Science 43 no. 4 (2002):569-579. https://doi.org/10.1080/0007166022000004480
Fischetti, V.A. “Bacteriophage endolysins: A novel anti-infective to control Gram-positive pathogens.” J Med Microbiol. 300 no. 6 (2010): 357–362. https://doi.org/10.1016/j.ijmm.2010.04.002
Gillor, O., A. Etzion and M.A. Riley. “The dual role of bacteriocins as anti- and probiotics.” Appl Microbiol Biotechnol. 81 no. 4 (2008): 591–606. https://doi.org/10.1007/s00253-008-1726-5
Hassan, J. O., and R. Curtiss III. “Virulent Salmonella typhimurium induced lymphocyte depletion and immunosuppression in chickens.” Infect. Immun. 62 (1994):2027–2036 https://doi.org/10.1128/IAI.62.5.2027-2036.1994
Hofacre, C.L., J.A. Smith, and G.F. Mathis. “Invited Review. An optimist’s view on limiting necrotic enteritis and maintaining broiler gut health and performance in today’s marketing, food safety, and regulatory climate.” Poultry Science 97 (2018):1929–1933. https://dx.doi.org/10.3382/ps/pey082
Jung, S.J., R. Houde, B. Baurhoo, X. Zhao, and B. H. Lee. “Effects of galacto-oligosaccharides and a bifidobacteria lactis-based probiotic strain on the growth performance and fecal microflora of broiler chickens.” Poultry Science 87 (2008):1694–1699. https://doi.org/10.3382/ps.2007-00489
Kaldhusdal and Skjerve. “Association between cereal contents in the diet and incidence of necrotic enteritis in broiler chickens in Norway.” Preventive Veterinary Medicine 28 (1996):1-16. https://doi.org/10.1016/0167-5877(96)01021-5
Keyburn, A. L., S. A. Sheedy, M. E. Ford, M. M. Williamson, M. M. Awad, J. I. Rood, and R. J. Moore. “Alpha-toxin of Clostridium perfringens is not an essential virulence factor in necrotic enteritis in chickens.” Infect. Immun. 74 (2006): 6496–6500. https://doi.org/10.1128/IAI.00806-06
Keyburn, A.L., J.D. Boyce, P. Vaz, T.L. Bannam, M.E. Ford, D. Parker, A. Di Rubbo, J.I. Rood, and R.J. Moore. “NetB, a new toxin that is associated with avian necrotic enteritis caused by Clostridium perfringens.” PLoS Pathog 4 no. 2, e26 (2008): 0001-0011. https://doi.org/10.1371/journal.ppat.0040026
Kim, G.-B., Y. M. Seo , C. H. Kim , and I. K. Paik. “Effect of dietary prebiotic supplementation on the performance, intestinal microflora, and immune response of broilers.” Poultry Science 90 (2011):75–82. https://doi.org/10.3382/ps.2010-00732
Knap, I., B. Lund, A. B. Kehlet, C. Hofacre, and G. Mathis. “Bacillus licheniformis prevents necrotic enteritis in broiler chickens.” Avian Diseases 54 no. 2 (2010):931-935. https://doi.org/10.1637/9106-101509-ResNote.1
Knarreborg, A., M.A. Simon, R.M. Engberg, B.B. Jensen, and G.W. Tannock. “Effects of Dietary Fat Source and Subtherapeutic Levels of Antibioticon the Bacterial Community in the Ileum of Broiler Chickensat Various Ages.” Applied and Environmental Microbiology 68 no. 12 (2002): 5918-5924. https://doi.org/0.1128/AEM.68.12.5918–5924.2002
Kocher, A. and M. Choct. “Improving broiler chicken performance. The efficacy of organic acids, prebiotics and enzymes in controlling necrotic enteritis.” Australian Government-Rural Industries Research and Development Corporation. Publ. no. 08/149 (2008).
https://www.agrifutures.com.au/wp-content/uploads/publications/08-149.pdf
Kondo, F. “In vitro lecithinase activity and sensitivity to 22 antimicrobial agents of Clostridium perfringens isolated from necrotic enteritis of broiler chickens.” Research in veterinary Science 45 (1988): 337-340. https://doi.org/10.1016/S0034-5288(18)30961-5
Kubena, L.F., J.A. Byrd, C.R. Young, and D.E. Corrier. “Effects of tannic acid on cecal volatile fatty acids and susceptibility to Salmonella typhimurium colonization in broiler chicks.” Poultry Science 80, no. 9 (2001): 1293–1298. https://doi.org/10.1093/ps/80.9.1293
Los, F.C.O., T.M. Randis, R.V. Aroian, and A.J. Ratner. “Role of pore-forming toxins in bacterial infectious diseases.” Microbiology and Molecular Biology Reviews 77 (2013): 173-207 https://doi.org/10.1128/MMBR.00052-12
M’Sadeq S.A., Shubiao Wu, Robert A. Swick, Mingan Choct. “Towards the control of necrotic enteritis in broiler chickens with in-feed antibiotics phasing-out worldwide.” Animal Nutrition 1 (2015): 1-11. https://dx.doi.org/10.1016/j.aninu.2015.02.004
Mathipa, M.G. and M.S. Thantsha. “Probiotic engineering: towards development of robust probiotic strains with enhanced functional properties and for targeted control of enteric pathogens.” Gut Pathog. 9 no. 28 (2017). https://doi.org/10.1186/s13099-017-0178-9
McDevitt, R.M., J.D. Brooker, T. Acamovic, and N.H.C. Sparks. “Necrotic enteritis, a continuing challenge for the poultry industry.” World’s Poultry Science Journal 62; World’s Poultry Science Association (June 2006). https://doi.org/10.1079/WPS200593
Miller, R.W., J. Skinner, A. Sulakvelidze, G.F. Mathis, and C.L. Hofacre. “Bacteriophage therapy for control of necrotic enteritis of broiler chickens experimentally infected with Clostridium perfringens.” Avian Diseases 54 no. 1 (2010): 33-40. https://doi.org/10.1637/8953-060509-Reg.1
Mitsch, P., K. Zitterl-Eglseer, B. Köhler, C. Gabler, R. Losa, and I. Zimpernik. “The Effect of Two Different Blends of Essential Oil Components on the Proliferation of Clostridium perfringens in the Intestines of Broiler Chickens.” Poultry Science 83 (2004):669–675. https://doi.org/10.1093/ps/83.4.669
Mitchell, A. “Choosing the right coccidiosis vaccine for layer and breeder chickens.” The Poultry Site March 21 (2017). https://thepoultrysite.com/articles/choosing-the-right-coccidiosis-vaccine-for-layer-and-breeder-chickens
Olkowski, A.A., C. Wojnarowicz, M. Chirino-Trejo, B. Laarveld, and G. Sawicki. “Sub-clinical necrotic enteritis in broiler chickens: Novel etiological consideration based on ultra-structural and molecular changes in the intestinal tissue.” Veterinary Science 85 (2008): 543–553. https://doi.org/10.1016/j.rvsc.2008.02.007
Pan, D. and Z. Yu. “Intestinal microbiome of poultry and its interaction with host and diet.” Gut Microbes 5 no. 1 (2014): 108–119. https://dx.doi.org/10.4161/gmic.26945
Porter, R., Jr. “Bacterial enteritides of poultry.” Poult. Sci. 77 (1998):1159–1165 https://doi.org/10.1093/ps/77.8.1159
Robert Koch Institut. “Grundwissen Antibiotikaresistenz“. https://www.rki.de/DE/Content/Infekt/Antibiotikaresistenz/Grundwissen/Grundwissen_inhalt.html#:~:text=Wenn%20ein%20neues%20Antibiotikum%20auf,%C3%BCberleben%20und%20vermehren%20sich%20weiter.
Rougière, N. and B. Carré. “Comparison of gastrointestinal transit times between chickens from D + and D- genetic lines selected for divergent digestion efficiency.” Animal 4 no. 11 (2010): 1861-1872. https://doi.org/10.1017/S1751731110001266
Santos, F.B.O., B.W. Sheldon, A.A. Santos Jr., and P.R. Ferket. ”Influence of housing system, grain type, and particle size on Salmonella colonization and shedding of broilers fed triticale or corn-soybean meal diets.” Poultry Science 87 (2008): 405-420. https://dx.doi.org/10.3382/ps.2006-00417
Schiavone, A. , K. Guo, S. Tassone, L .Gasco, E. Hernandez, R. Denti, and I. Zoccarato. “Effects of a Natural Extract of Chestnut Wood on Digestibility, Performance Traits, and Nitrogen Balance of Broiler Chicks.” Poult Sci. 87 no. 3 (2008): 521-527. https://doi.org/10.3382/ps.2007-00113
Shivaramaiah, S., R. E. Wolfenden, J. R. Barta, M. J. Morgan, A. D. Wolfenden, B. M. Hargis, and G. Téllez. „The role of an early Salmonella typhimurium infection as a predisposing factor for necrotic enteritis in a laboratory challenge model.” Avian Diseases 55 (2011): 319-323. https://doi.org/10.1637/9604-112910-ResNote.1
Singh, Y., V. Ravindran, T.J. Wester, A.L. Molan, and G. Ravindran. “ Influence of feeding coarse corn on performance, nutrient utilization, digestive tract measurements, carcass characteristics, and cecal microflora counts of broilers.” Poultry Science 93 (2014): 607–616. https://dx.doi.org/10.3382/ps.2013-03542
Skrivanova, E., M. Marounek, V. Benda, and P. Brezina. “Susceptibility of Escherichia coli, Salmonella sp. and Clostridium perfringens to organic acids and monolaurin.” Veterinarni Medicina 51 no. 3 (2006): 81–88. https://doi.org/10.17221/5524-VETMED
Songer, J.G. “Clostridial Enteric Diseases of Domestic Animals.” Clinical Microbiology Reviews 9 no. 2 (1996): 216-234. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC172891/pdf/090216.pdf
Stanley D., Wu S.-B., Rodgers N., Swick R.A., and Moore R.J. “Differential Responses of Cecal Microbiota to Fishmeal, Eimeria and Clostridium perfringens in a Necrotic Enteritis Challenge Model in Chickens.” PLoS ONE 9 no. 8 (2014): e104739. https://doi.org/10.1371/journal.pone.0104739
Tan, L., D. Rong, Y. Yang, and B. Zhang. “Effect of Oxidized Soybean Oils on Oxidative Status and Intestinal Barrier Function in Broiler Chickens.” Brazilian Journal of Poultry Science 18 no. 2 (2018): 333-342. http://dx.doi.org/10.1590/1806-9061-2017-0610
Tan, L., D. Rong, Y. Yang, and B. Zhang. “The Effect of Oxidized Fish Oils on Growth Performance, Oxidative Status, and Intestinal Barrier Function in Broiler Chickens.” J. Appl. Poult. Res. 28 (2019): 31-41. http://dx.doi.org/10.3382/japr/pfy013
ThePoultrySite. “Necrotic Enteritis. Disease Guide”. https://thepoultrysite.com/disease-guide/necrotic-enteritis
Timbermont L., A. Lanckriet, J. Dewulf, N. Nollet, K. Schwarzer, F. Haesebrouck, R. Ducatelle, and F. Van Immerseel. “Control of Clostridium perfringens-induced necrotic enteritis in broilers by target-released butyric acid, fatty acids and essential oils.” Avian Pathol. 39 no. 2 (2010): 117-21. https://doi.org/10.1080/03079451003610586
Tsiouris, V. “Poultry management: a useful tool for the control of necrotic enteritis in poultry.” Avian Pathol. 45 no. 3 (2016):323-325. https://doi.org/10.1080/03079457.2016.1154502
Van der Most, P.J., B. de Jong, H.K. Parmentier and S. Verhulst. “Trade-off between growth and immune function: a meta-analysis of selection experiments.” Functional Ecology 25 (2011): 74-80. https://doi.org/0.1111/j.1365-2435.2010.01800.x
Van der Sluis, W. “Clostridial enteritis is an often underestimated problem.” Worlds Poult. Sci. J. 16 (2000):42–43.
Van der Suis, W. “Necrotic enteritis kills birds and profits.” Poultry World Apr5 (2013). https://www.poultryworld.net/Health/Articles/2013/4/necrotic-enteritis-kills-birds-and-profits-1220877W/
Van Immerseel, F., J. De Buck, F. Pasmans, G. Huyghebaert, F. Haesebrouck, and R. Ducatelle. “Clostridium perfringens in poultry: an emerging threat of animal and public health.” Avian Pathology 33 (2004): 537-549. https://doi.org/10.1080/03079450400013162
Van Immerseel, F., J.I. Rood, R.J. Moore, and R.W. Titball. “Rethinking our understanding of the pathogenesis of necrotic enteritis in chickens.” Trends in Microbiology 17 no. 1 (2008):32-36. https://doi.org/10.1016/j.tim.2008.09.005
Wade, B., A. Keyburn. “The true cost of necrotic enteritis.” World Poultry 31 no. 7 (2015): 16–17. https://www.poultryworld.net/Meat/Articles/2015/10/The-true-cost-of-necrotic-enteritis-2699819W/
Wade, B., A.L. Keyburn, T. Seemann, J.I. Rood, and R.J. Moore. “Binding of Clostridium perfringens to collagen correlates with the ability to cause necrotic enteritis in chickens.” Veterinary Microbiology 180 no. 3–4 (2015): 299-303. https://doi.org/10.1016/j.vetmic.2015.09.019
Williams, R.B. “Intercurrent coccidiosis and necrotic enteritis of chickens: rational, integrated disease management by maintenance of gut integrity.” Avian Pathology 34 no. 3 (2005):159-180. https://doi.org/10.1080/03079450500112195
Yang , C.M., G.T. Cao, P.R. Ferket, T.T. Liu, L. Zhou, L. Zhang, Y.P. Xiao, and A. G. Chen. “ Effects of probiotic, Clostridium butyricum, on growth performance, immune function, and cecal microflora in broiler chickens.” Poultry Science 91 (2012): 2121–2129. https://dx.doi.org/10.3382/ps.2011-02131
